马上注册,阅读更多内容,享用更多功能!
您需要 登录 才可以下载或查看,没有账号?立即注册 
×
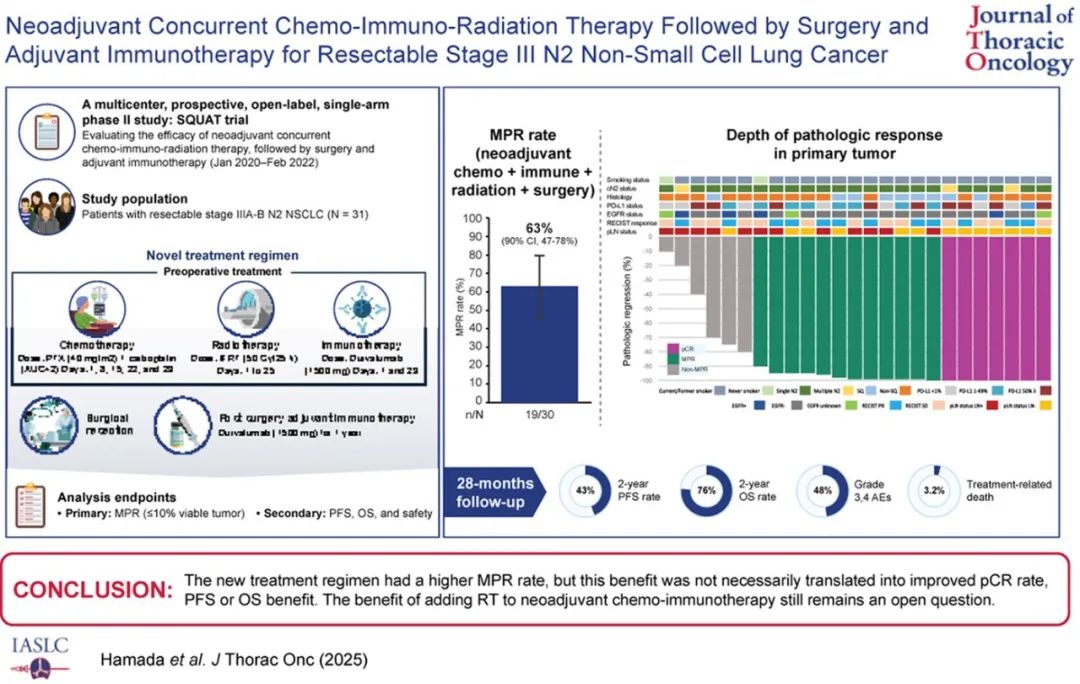

引言 新辅助化学免疫治疗已成为可切除的II至III期非小细胞肺癌(NSCLC)的一项标准治疗方案。然而, CheckMate 816研究结果显示,其在局部控制方面仍存在不足,提示肿瘤局部复发风险仍然较高。基于此,我们推测,在新辅助治疗中联合放疗可能有助于提升局部控制率,进而改善患者的长期生存结局。 方法 本研究纳入符合以下标准的患者:临床分期为T1至T3或T4(指肿瘤体积),N2期,IIIA至IIIB期NSCLC(依据美国癌症联合委员会第8版分期标准),且经病理证实无N2结外侵犯。所有患者接受同步放化疗联合免疫治疗:化疗方案为卡铂(AUC=2)联合紫杉醇(40 mg/m²),分别于第1、8、15、22和29天给药;同时给予总剂量为50 Gy的放射治疗,在25天内完成。免疫治疗采用度伐利尤单抗(1500 mg),在第1天和第29天各给予一次。同步治疗结束后2至6周内实施外科切除术,术后继续给予度伐利尤单抗作为辅助治疗,最长可持续1年。 主要研究终点为主要病理反应率(MPR,定义为残存活肿瘤≤10%);次要终点包括病理完全缓解率(pCR)、无进展生存期(PFS)、总生存期(OS)及安全性。 结果 自2020年1月至2022年2月,共有来自日本10家医疗机构的31例患者入组本研究。结果显示,MPR率为63%(90%置信区间:47%–78%),达到预设的主要终点,病理完全缓解率为23%。中位随访时间为28个月,2年无进展生存率(PFS)为43%,总生存率(OS)为76%。共有48%的患者发生了3级或4级不良事件,其中1例为治疗相关死亡。 结论 相比近期其他围手术期化学免疫治疗研究,本研究方案取得了更高的MPR率,提示同步放化疗联合免疫治疗可能具有较强的肿瘤控制潜力。然而,该局部反应优势尚未显著转化为PFS或OS的改善,仍需进一步随访与研究加以验证。 引言近年来,新辅助或围手术期化学免疫治疗已成为无驱动基因突变的可切除 II 至 III 期非小细胞肺癌(NSCLC)患者的标准治疗策略之一。CheckMate 816 研究首次证实,新辅助 nivolumab 联合含铂双药化疗可显著提高病理完全缓解率(pCR)并改善无事件生存期(EFS),总生存期(OS)亦呈现良好趋势。此外,多个后续试验进一步验证了围手术期策略(即在新辅助免疫治疗基础上追加辅助免疫治疗)的潜在益处。值得注意的是,CheckMate 816 试验结果显示,免疫治疗虽显著降低了远处复发率(从22%降至10%),但局部区域复发率在免疫治疗组与对照组之间差异不大(22% vs. 19%)。这一现象提示,单纯免疫治疗在局部控制方面可能仍存在不足。 既往研究表明,放射治疗(RT)除具备局部杀伤肿瘤的能力外,还可调节肿瘤微环境,增强免疫应答,在一定条件下甚至可诱导远处抗肿瘤作用(“放射免疫协同效应”)。因此,我们推测将RT纳入新辅助化学免疫治疗,可能进一步改善局部控制并提升全身疗效。 基于此假设,我们开展了SQUAT试验(WJOG 12119L)——一项多中心、前瞻性、单组II期研究,旨在评估可切除 III-N2 期 NSCLC 患者接受新辅助同步化疗-免疫-放疗后联合手术与辅助免疫治疗的可行性、有效性及安全性。 材料与方法研究设计与患者招募SQUAT试验为多中心、开放标签、单组II期临床试验。纳入标准包括: 所有患者均签署书面知情同意书。由于研究启动时尚未公布 ADAURA 和 ALINA 试验结果,允许 EGFR突变或ALK易位的患者入组。排除标准包括活动性自身免疫病(需系统性免疫抑制治疗者)、活动性间质性肺病、妊娠及其他严重合并症等。研究符合《赫尔辛基宣言》并获各中心伦理委员会批准(注册号:JapicCTI-195069)。 新辅助阶段:患者于第1、8、15、22、29天接受每周卡铂(AUC=2)联合紫杉醇(40 mg/m²)化疗,并同时进行25次、总剂量为50 Gy的局部放射治疗(肺V20 < 35%,平均剂量 < 20 Gy)。第1天与第29天静脉注射度伐利尤单抗(1500 mg)。 重新评估与手术:放疗结束后2–6周内,复查CT、PET/CT及(必要时)脑MRI/CT以重新评估肿瘤可切除性。随后实施肺叶切除术或全肺切除术并行系统性纵隔淋巴结清扫。 辅助治疗:确诊手术后,于术后每4周给予度伐利尤单抗1500 mg,最长持续12个月。
分期与检测所有患者入组前均接受CT、PET/CT、脑MRI或CT检查,N2状态需通过支气管镜下针吸活检、纵隔镜检查或胸腔镜活检确认。PD-L1表达使用SP263抗体进行评估,EGFR/ALK状态检测非强制要求。 终点设定PFS 定义为自登记起至不可切除进展、术后复发、疾病进展或全因死亡的时间;OS定义为登记至死亡时间。未发生事件者于最后随访日数据截尾。 随访与安全性评估术后随访计划为术后首年每12周一次,次年起每24周一次,常规CT复查,脑部影像每年一次。PET/CT视情况使用。不良事件依据NCI CTCAE v5.0标准进行分级和记录。 结果患者与治疗情况自2020年1月至2022年2月,共纳入来自日本10家机构的31例患者,纳入安全性分析集(SAS)评估不良事件。由于1例患者注册后被认定为不符合纳入标准,共有30例患者被纳入意向性治疗集(ITT)评估疗效,其中25例进一步纳入符合方案集(PPS)(见补充图2)。 30例患者中,70%为临床分期IIIA期,63%为非鳞癌组织学类型(表1)。所有患者术前均确诊为N2淋巴结阳性,诊断手段包括支气管内超声引导针吸活检(77%,28例)、纵隔镜检查(10%,3例)和胸腔镜活检(13%,4例)。
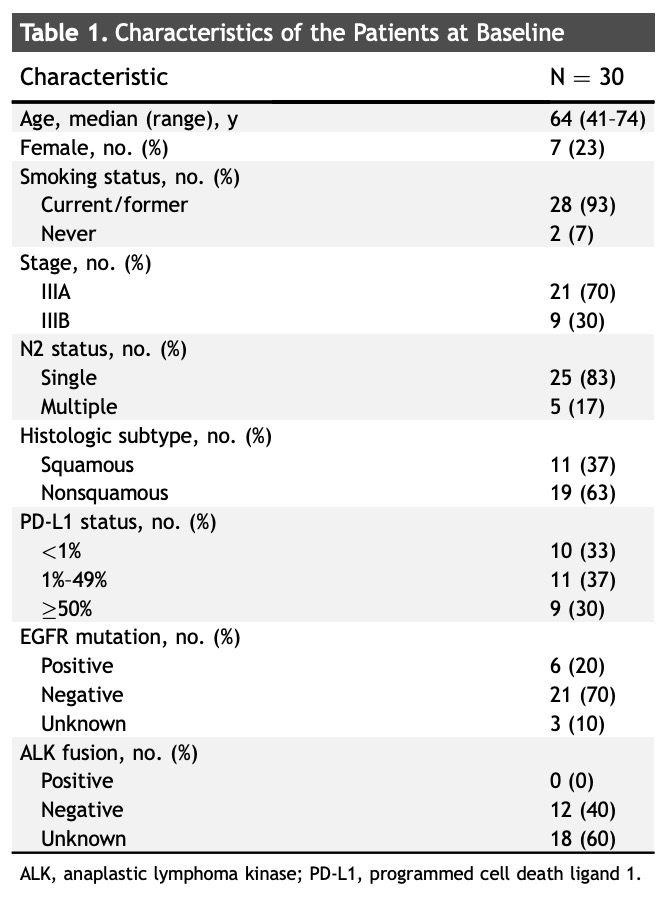
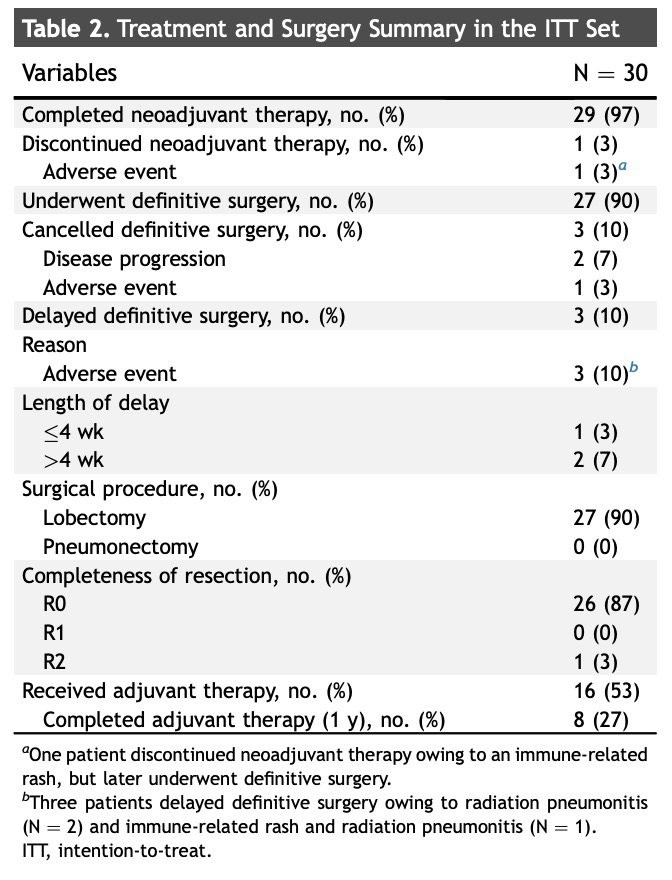
其中29例(97%)患者完成了全部新辅助治疗方案(表2),新辅助度伐单抗治疗的中位周期为2个周期(四分位距[IQR]:2–2)。30例中有16例(53%)进入辅助度伐单抗治疗阶段,但仅8例(27%)完成了一年的治疗。辅助治疗的中位周期为12个周期(IQR:6–14),未完成一年的原因包括疾病复发(6例)和不良事件(2例)。
 手术情况
手术情况初始入组的13例患者中有11例完成新辅助治疗并成功接受后续手术,未触发提前终止标准。ITT组中90%(27/30)接受了计划性手术。未能接受手术的3例中,2例因疾病进展,1例因不良事件。 因不良事件(放射性肺炎2例、免疫相关皮疹合并放射性肺炎1例),3例(10%)患者的手术被推迟超过6周。3例中1例为CTCAE 2级放射性肺炎,2例为1级。术后手术中位延迟时间为28天。 所有接受手术的患者均行肺叶切除术,其中87%(26/30)达到了R0切除,1例因术中发现胸膜播散而为R2切除,并接受奥希替尼治疗(该患者为EGFR突变阳性)。 疗效评估ITT组的主要病理缓解(MPR)率为63%,接近预设目标MPR率65%,90%置信区间(CI)下限为47%,超过阈值40%,达到研究主要终点(图1A)。PPS和去除EGFR突变患者后的PPS中MPR率分别为76%(95% CI:55%–91%)和81%(95% CI:58%–95%)(补充图3A)。完全病理缓解(pCR)率分别为:ITT组23%、PPS组28%、EGFR阴性PPS组29%(图1A、补充图3B)。
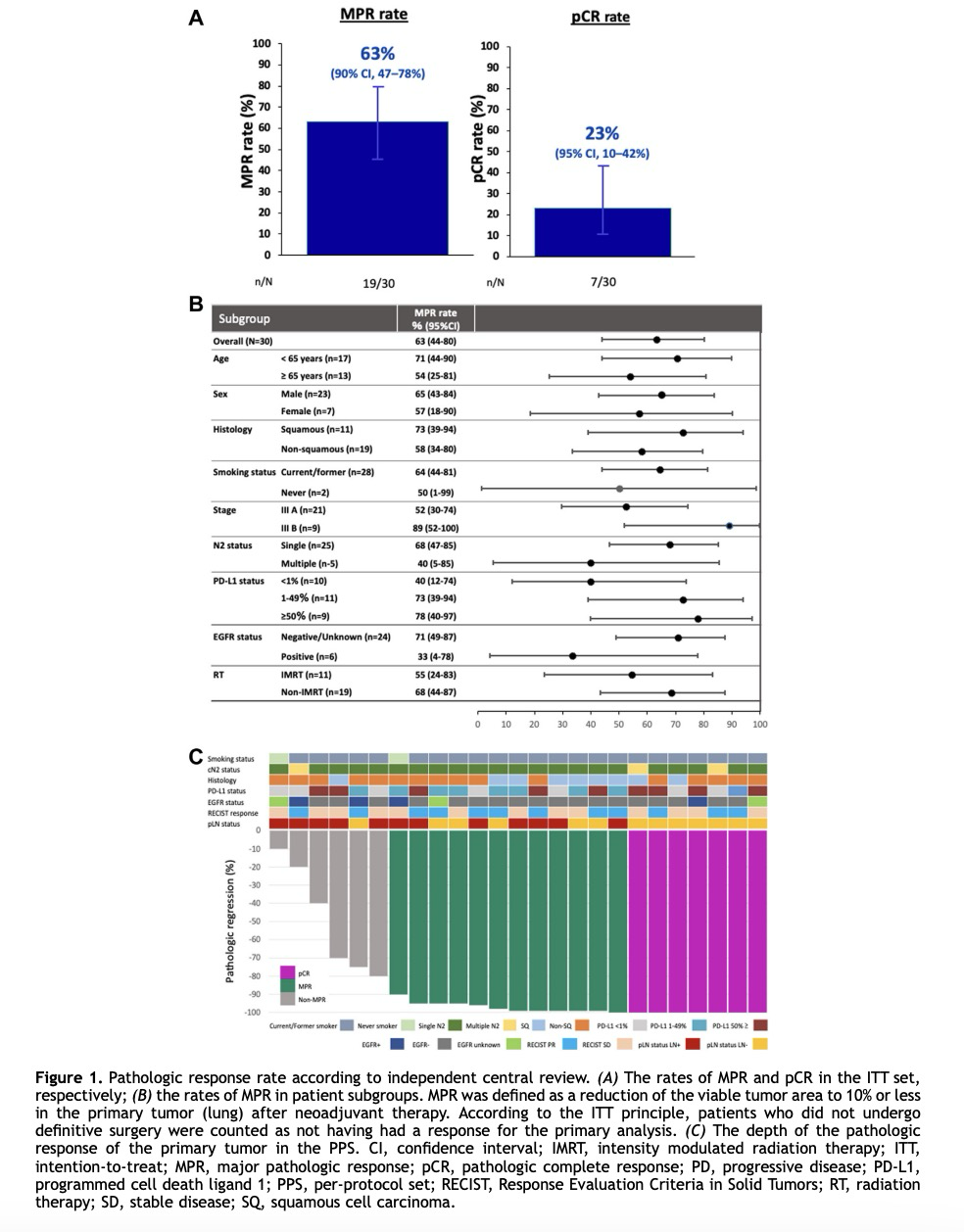
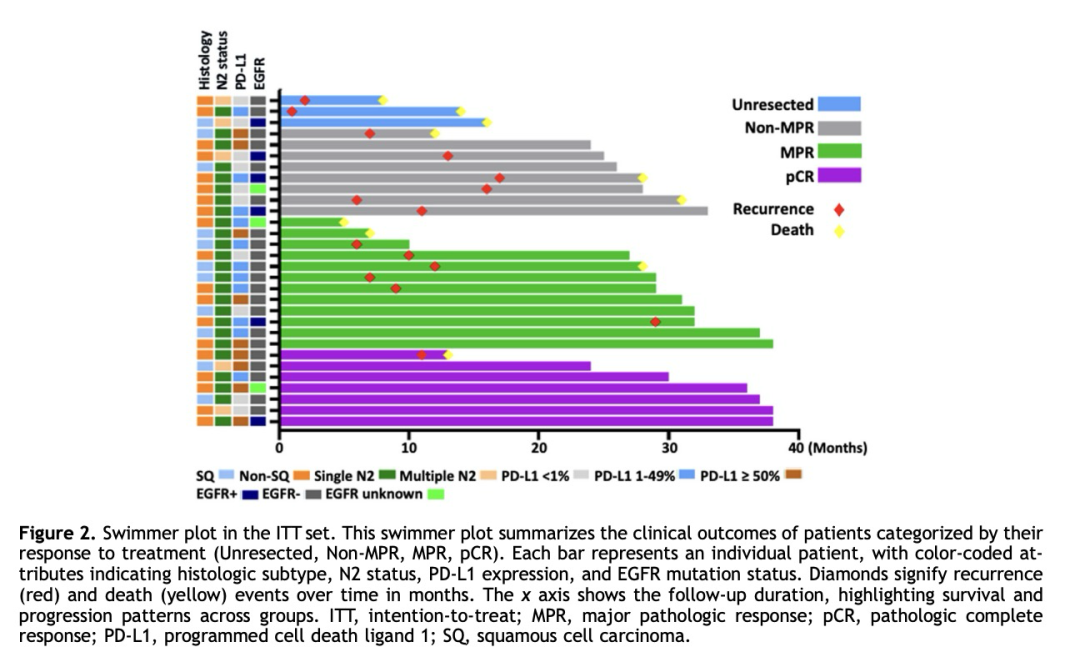
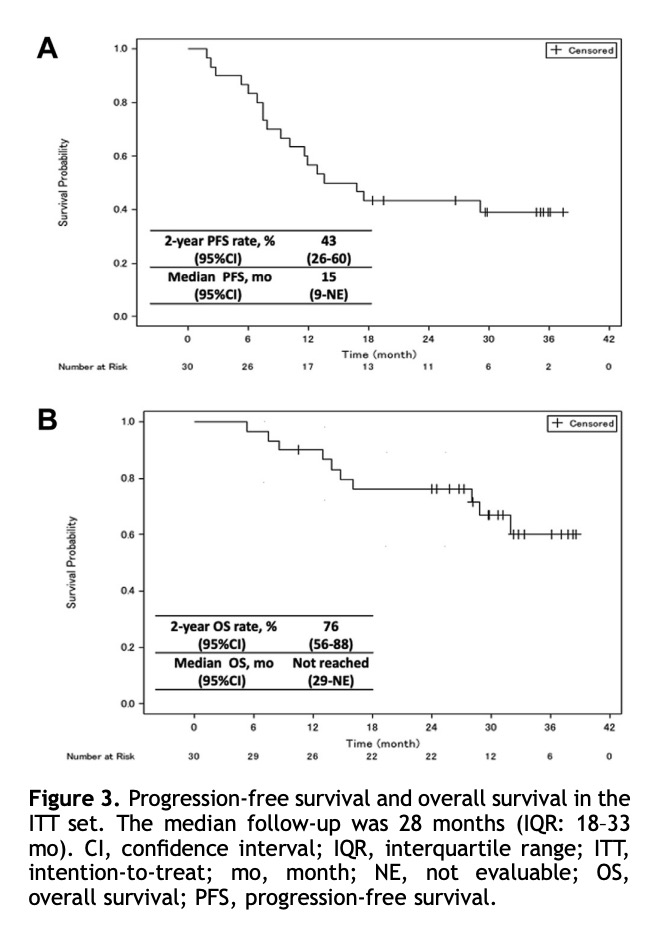
亚组分析显示:IIIB期、单站N2、PD-L1阳性及EGFR阴性患者MPR率较高(图1B);IIIB期、多站N2、PD-L1≥50%、EGFR阴性患者pCR率较高(补充图4)。与既往全球新辅助/围手术期研究结果1–7相比,PPS中原发肿瘤的病理缓解深度较理想(图1C)。ITT组的客观缓解率(ORR)为47%(14/30)(补充图5)。 中位随访时间为28个月(IQR:18–33个月)。ITT组中15例(50%)复发,10例(33%)死亡(图2)。中位无进展生存期(PFS)为15个月(95% CI:9–未成熟),中位总生存期(OS)尚未达到。2年PFS和OS率分别为43%(95% CI:26%–60%)和76%(95% CI:56%–88%)(图3)。PPS组2年PFS率和OS率分别为48%(95% CI:28%–66%)和84%(95% CI:62%–94%)(补充图6)。
6例EGFR突变患者中,4例发生复发,其中3例接受奥希替尼治疗。探索性分析显示,达成MPR的患者PFS和OS均优于未达成者(2年PFS率:58% vs. 18%;2年OS率:84% vs. 64%)(补充图7)。类似趋势亦见于pCR患者(补充图8)。
复发模式包括:局部复发2例(7%)、局部合并远处复发4例(13%)、单纯远处复发9例(30%)。所有局部复发均发生于放射野内。最常见的远处复发部位为脑(6例,20%)(补充表1)。 安全性和手术相关并发症所有SAS患者(31/31)均发生过至少一种不良事件(表3)。治疗相关3–4级不良事件发生率为48%(15/31),最常见为3–4级中性粒细胞减少症(23%,7/31)。有3例(10%)因治疗相关不良事件提前终止治疗。
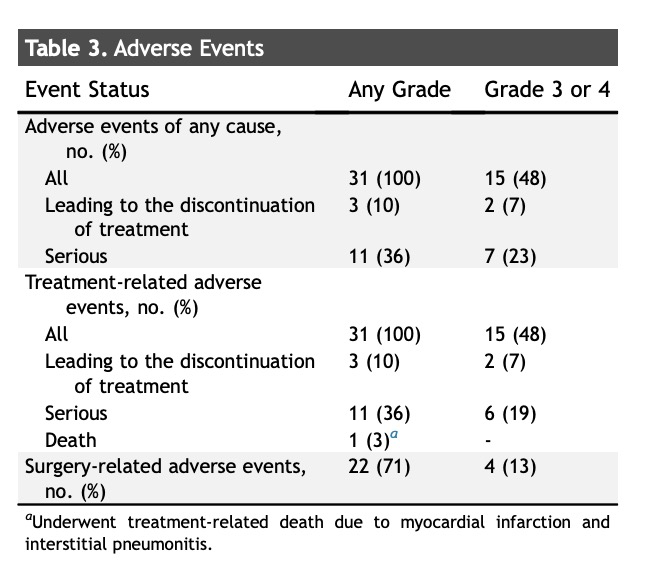
免疫相关不良事件总体发生率较低,但1例患者在手术后出现免疫相关性肺炎和心肌梗死,虽经导尿及类固醇治疗仍死亡。 手术并发症方面,22例(71%)发生任一等级的手术不良事件,4例(13%)为3–4级手术不良事件。放射性肺炎在8例(26%)中出现,未观察到支气管胸膜瘘。 讨论 本研究结果显示,MPR 率高达 63%,几乎是近年四项全球新辅助/围手术期 III 期 NSCLC 研究中报告的 MPR 率(30%–37%)的两倍。尽管结果令人鼓舞,但应谨慎解读,因为 II 期临床研究中的患者选择标准更为严格,往往存在疗效高估的风险。例如,NADIM 和 NADIM II 研究中 MPR 率分别为 83% 和 53%,两者均采用了围手术期 nivolumab 治疗。这些研究提示,在新辅助化疗-免疫治疗基础上增加放疗,可能有助于提高 III 期 N2 NSCLC 的局部控制率。 然而,值得注意的是,尽管 MPR 率较高,本研究中两年 PFS 和 OS 率分别仅为 43% 和 76%;48% 的患者出现 3–4 级不良事件,并有 1 例治疗相关死亡,提示治疗毒性不容忽视。 目前,放疗与新辅助化学免疫治疗联合用于 II–III 期 NSCLC 的研究报道仍较有限,仅有三项研究公开相关数据。其中一项采用 帕博利珠单抗联合放化疗治疗 III 期 N2 NSCLC 的研究因不良事件频发被提前终止,其安全性仍有争议。另两项研究仍在进行中,INCREASE 试验中报道的 MPR 和 pCR 分别为 79% 和 63%,而另一项与本研究治疗方案相似的研究中,MPR 和 pCR 分别为 78% 和 39%。尽管病理缓解结果良好,但这些研究尚未公布长期随访数据。 在我们的研究中,MPR 率虽显著提高,但 pCR 率为 23%,与其他新辅助/围手术期研究中报道的 17%–25% 相当。此外,两年 PFS 为 43%(95% CI:26%–60%),OS 为 76%(95% CI:56%–88%),略低于其他研究中 EFS(62%–64%)和 OS(79%–82%)的数据差异,可能部分源于我们研究中仅纳入 III 期 N2 患者,且新辅助化疗-免疫治疗周期数较少(2 个周期),而多数研究为 3–4 个周期。为了降低放疗相关毒性,本研究减少了新辅助治疗强度,但可能影响了系统性控制效果。 复发模式也提示了这一点。在 15 例复发中,有 13 例为远处转移,其中 6 例为脑转移,仅 2 例为局部复发(见补充表 1)。与 CheckMate 816 试验中 43 例复发中仅 15 例为远处复发(其中脑转移 6 例)相比,我们的远处控制能力较差,可能与免疫治疗周期较少有关。 此外,本研究中接受术后辅助免疫治疗的患者比例为 53%,低于其他研究报告的 62%–73%,可能与放射相关毒性限制治疗依从性有关。值得注意的是,放化疗期间同步加入免疫治疗是否获益仍存争议。 PACIFIC-2 研究显示,在不可切除的 III 期 NSCLC 中,放化疗同步 ICI 并未显著优于单独放化疗,这与我们研究中的结果一致,即新辅助放化疗同步免疫治疗未必优于单独的新辅助放化疗。 结论 我们开展了一项单组 II 期临床试验,探索新辅助化疗-免疫-放疗联合根治性手术及术后免疫治疗在 III 期 N2 NSCLC 患者中的疗效。尽管该方案显著提高了 MPR 率,但并未转化为 pCR、PFS 或 OS 的明确改善。这可能与新辅助治疗强度偏低有关。是否在新辅助化疗-免疫治疗基础上加用放疗能够带来真正获益,仍需更多随机对照研究验证。此外,延长随访时间以观察长期疗效也至关重要。 |