处理
1. 标本前处理:手术切除标本(包括肺楔形切除、肺段切除、肺叶切除、左/右全肺切除)应遵循病理规范化诊断总则要求,尽量在半小时以内将标本剖开固定,选用足量的10%中性缓冲福尔马林固定液浸泡标本,固定时间12~48 h,不超过72 h(强烈推荐)。
2. 标本记录及取材:手术切除标本病理取材前应尽量参考患者CT和气管镜等临床检查,以防止遗漏重要病变或小病灶。观察并记录手术切除标本类型、肿瘤大小、边界、质地和脏层胸膜情况,同时须注意观察周围肺是否有阻塞性炎性改变或伴发其他肺结节,以及肿物与胸膜和手术切缘的关系。取材数量必须满足病理诊断需求,若肿物最大径≤3 cm,应全部取材;若肿物最大径>3 cm,每增加1 cm至少增加1块取材。由于肿物最大径与TNM分期直接相关,准确测量肿瘤最大径具有重要临床意义。肿物大小可根据新鲜标本或固定后标本进行测量,测量要求精确到1 mm,需注意分期的阈值1 cm、2 cm、3 cm、4 cm、5 cm和7 cm。若肿物紧贴脏层胸膜,需在可疑脏层胸膜侵犯处取材。中央型肿物需要描述距支气管切缘距离及与支气管的关系。肺楔形切除标本还需描述肿物距肺切缘的距离,并取距离最近处肺切缘。当肿物邻近切缘时,应注意采用垂直切缘取材而非平行切缘侧取材。外科送检淋巴结应全部按分组取材,对于叶切标本如有第12组淋巴结(肺内支气管旁淋巴结)时应当予以取材。
病理学评估
肺癌手术切除标本病理诊断总体原则(强烈推荐)是应满足临床分期及诊治需要,包括肿瘤大小、脉管癌栓、神经侵犯、胸膜侵犯、手术切缘情况、气腔内播散(spread through air spaces, STAS)及淋巴结转移等(强烈推荐)。根据美国癌症联合委员会(American Joint Committee on Cancer, AJCC)/国际肺癌研究协会(International Association for the Study of Lung Cancer, IASLC)第8版或第9版分期系统进行术后病理分期(pTNM)。
手术标本诊断术语依据第5版《WHO肺部肿瘤组织学分类》(强烈推荐),肺癌病理组织学分型包括腺癌、鳞状细胞癌、腺鳞癌、大细胞癌和肉瘤样癌、神经内分泌肿瘤(小细胞癌、大细胞神经内分泌癌、类癌)、涎腺型癌及其他一些少见类型恶性肿瘤等。具体组织学亚型及常见评估指标诊断原则如下。
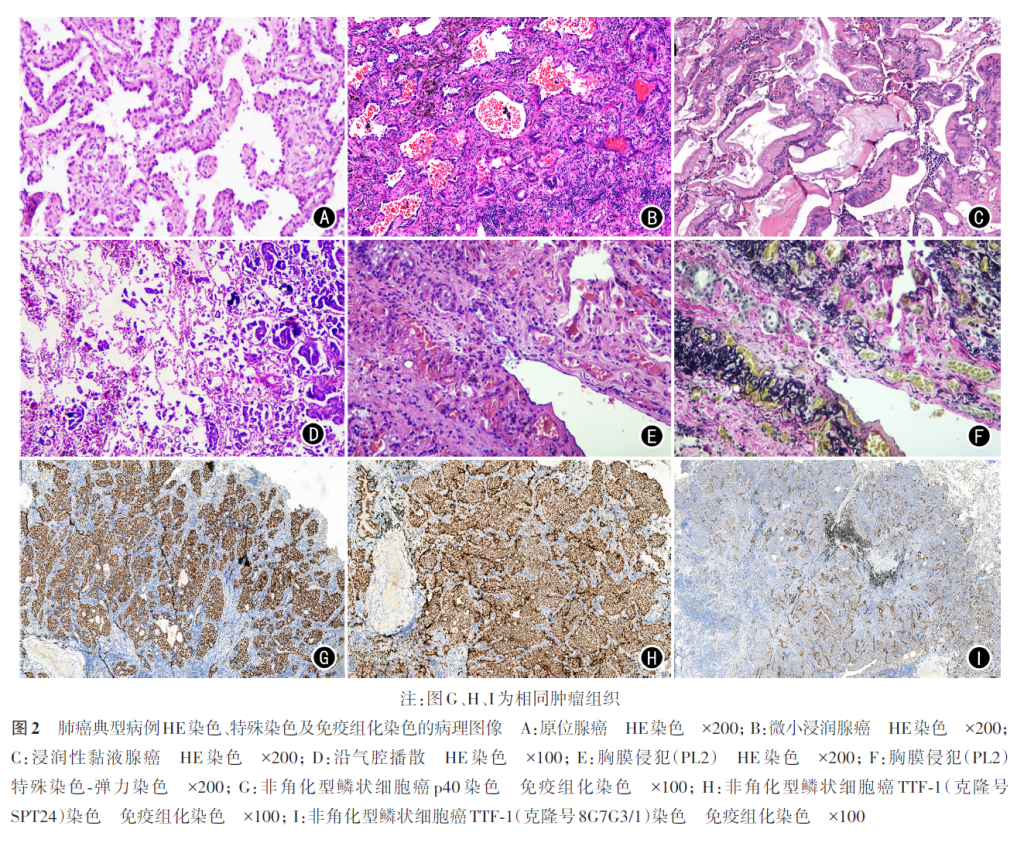
1. 腺癌及其前驱病变:前驱病变包括非典型腺瘤样增生和原位腺癌(图2A),主要形态鉴别点在于细胞异型性和细胞增生的密集程度。前者轻度异型性,细胞稀疏排列不连续,病变范围小,常≤5 mm,但5 mm大小不是诊断的必须条件;后者分为非黏液型(多见)和黏液型(少见),细胞轻度至中度异型性,连续单层排列,偶尔可见细胞重叠或轻微复层,缺乏核分裂像,肿瘤最大径≤30 mm。非典型腺瘤样增生和原位腺癌的诊断是基于肿瘤完全取材后进行充分病理评估的结果,活检标本及细胞学标本不能直接诊断,术中冰冻诊断也会存在诊断局限性(强烈推荐)。
腺癌包括微小浸润性腺癌(浸润灶≤5 mm,分为非黏液型和少见的黏液型)、浸润性非黏液腺癌、浸润性黏液腺癌、胶样腺癌、胎儿型腺癌和肠型腺癌(强烈推荐)。非黏液型微小浸润腺癌(图2B)应与肺泡扩张不良造成的肺泡塌陷进行鉴别,主要鉴别点为类似腺泡状的塌陷肺泡上皮与扩张良好的单层排列的肺泡上皮形态相似,肺泡间隔增宽不是由增生的癌性肌纤维母细胞成分造成,上皮结构缺乏典型的腺泡型、乳头型或其他高级别浸润亚型。黏液型微小浸润腺癌少见,以贴壁排列的异型性较小的高柱状黏液上皮为主并出现结构紊乱或明确肌纤维母细胞间质中的浸润成分,且范围≤5 mm。
浸润性非黏液腺癌常见亚型包括贴壁型、腺泡型、乳头型、微乳头型和实体型,常为多个亚型混合存在。病理诊断以5%为增量单位记录不同亚型所占比例,从高至低依次列出(弱推荐)。肺浸润性非黏液性腺癌的IASLC新分级系统根据主要亚型及有无20%及以上的高级别成分(包括实性、微乳头、筛状和/或复杂腺体成分)将腺癌分为三级,即高(G1)、中(G2)、低(G3)分化腺癌。该三级分类对于肺浸润性非黏液腺癌患者的预后预测价值优于主要组织学亚型的分级系统。由于各亚型占比重复性较差,推荐组织学分级作为诊断的重要内容(强烈推荐)。
肺浸润性黏液腺癌(图2C)主要背景特点是贴壁排列的杯状或柱状黏液上皮,核小位于基底部,轻度核异型性或缺乏核异型性,浸润成分可以是腺泡状、乳头状、微乳头状、实性和筛状结构等。
2. 鳞状细胞癌及其前驱病变:前驱病变包括鳞状上皮异型增生(轻、中、重度)和原位鳞状细胞癌。鳞状细胞癌包括角化型鳞状细胞癌、非角化型鳞状细胞癌、基底细胞鳞状细胞癌和淋巴上皮癌四个亚型。淋巴上皮癌是一类伴有不等量的淋巴浆细胞浸润的鳞状细胞癌,常与EBV感染有关。肺鳞状细胞癌需要与肺原发性涎腺肿瘤、SMARCA4缺失的未分化肿瘤、NUT癌及转移性尿路上皮癌、胸腺癌等肿瘤鉴别。
3. 腺鳞癌:含有腺癌和鳞状细胞癌两种成分,每种成分占全部肿瘤比例≥10%,因此该亚型须在手术切除标本中方可诊断(强烈推荐)。
4. 大细胞癌:未分化NSCLC,诊断时形态学必须先排除鳞状细胞癌、腺癌、大细胞神经内分泌癌及其他NSCLC亚型组织学特征,免疫组化及黏液染色亦不支持鳞、腺分化。大细胞癌需要手术切除标本充分取材后才能诊断,活检标本、冰冻切片(取材有限)、细胞学标本和转移灶标本均不宜诊断大细胞癌(强烈推荐)。
5. 肉瘤样癌:分为多形性癌、肺母细胞瘤及癌肉瘤三个亚型,而多形性癌又包括既往的巨细胞癌和梭形细胞癌亚型。其中肉瘤样成分需占肿瘤的10%及以上方可诊断多形性癌。
6. 神经内分泌肿瘤:包括典型类癌、不典型类癌、小细胞癌和大细胞神经内分泌癌。低级别的典型类癌和中等级别的非典型类癌相当于神经内分泌肿瘤(neuroendocrine tumor, NET) 1级(G1)和2级(G2),小细胞癌和大细胞神经内分泌癌又称之为高级别神经内分泌癌(neuroendocrine carcinoma,NEC)。值得注意的是,伴高增殖活性/核分裂增多的非典型类癌组织学形态类似于非典型类癌,但核分裂像(>10/2 mm2)和/或Ki-67指数>30%,相当于神经内分泌肿瘤3级(NET,G3),该类肿瘤分子遗传学更接近于类癌(MEN1突变),而不同于大细胞神经内分泌癌/小细胞癌(TP53、RB1共突变为主)。该类肿瘤原发在肺极为罕见,暂不推荐诊断。
核分裂及坏死指标是神经内分泌肿瘤分类的主要指标(强烈推荐),具体为典型类癌:核分裂像<2个/2 mm2,无坏死;不典型类癌:核分裂像(2~10个)/2 mm2,和/或小灶或点状坏死;高级别神经内分泌癌:核分裂像>10个/2 mm2,和/或大片坏死。目前与消化系统的神经内分泌肿瘤分类标准不同,Ki-67不是诊断肺神经内分泌肿瘤亚型的必需指标,但对其分级极为重要,特别是活检样本中鉴别NETs和NEC至关重要(强烈推荐)。
7. 肺涎腺肿瘤:包括多形性腺瘤、黏液表皮样癌、腺样囊性癌、上皮⁃肌上皮癌及涎腺型玻璃样变透明细胞癌等。玻璃样变透明细胞癌是一种极为少见的涎腺型低度恶性肿瘤,起源于气管、支气管黏膜下小涎腺,临床常常引起阻塞性症状,肿瘤呈惰性生长,几乎不复发。肺的涎腺型肿瘤与头颈部发生的涎腺肿瘤的组织病理学形态及分子遗传学相似。
8. 胸部SMARCA4缺失性未分化肿瘤:具有高度恶性生物学行为,患者通常为年轻至中年男性吸烟者。组织学上该类肿瘤的由弥漫、失黏附性、大而圆的上皮样细胞组成,肿瘤细胞胞质丰富,空泡状核,核仁明显。肿瘤中可局灶性出现横纹肌样细胞,较易出现核分裂像及坏死。罕见表现包括梭形、黏液变、硬化、肺泡样、透明细胞变。免疫组化典型病例表现为SMARCA4(BRG1)表达完全缺失,约有25%的病例表现为SMARCA4染色弥漫性减弱,同时常伴随SMARCA2(BRM)染色缺失并表达SMARCB1(INI1)蛋白。许多病例可伴有CD34、SOX2、SALL4、Syn阳性,p53常过表达,肿瘤细胞CK表达局灶或弱阳性,通常不会弥漫性表达Claudin4、p63、TTF-1、p40、WT-1。值得注意的是约有5%的NSCLC病例可出现SMARCA4缺失,可通过其典型的腺、鳞状细胞癌形态结构及免疫组化表达(如广谱CK弥漫强阳)情况加以鉴别,切记勿将SMARCA4缺失的肺癌误诊为SMARCA4缺失的未分化肿瘤(推荐)。另外胸外其他脏器亦可发生SMARCA4缺失的肿瘤,需注意与其他部位的转移肿瘤相鉴别。
9. STAS:9版AJCC 癌症分期系统STAS(图2D)定义为肺癌肿瘤细胞出现在主瘤灶以外周围肺实质的第一层及/或以外肺泡腔内,诊断需≥2个独立细胞簇并排除人为假象,可表现为微乳头、实性巢状或单个游离细胞3种形式(推荐)。由于存在假阴性及假阳性分类风险,目前冰冻诊断尚不推荐常规报告STAS;腺癌是STAS最常见病理类型,其他肺癌病理类型如鳞状细胞癌、腺鳞癌、大细胞癌及神经内分泌癌等也可存在STAS。STAS作为第9版AJCC TNM分期补充组织学描述,目前尚未直接用于T分期调整内容。
10. 胸膜侵犯(强烈推荐):胸膜是否受侵以及侵犯程度与T分期密切相关。肿瘤破坏胸膜弹力纤维层,或肿瘤侵达脏层胸膜表面定义为脏层胸膜受侵(图2E、F),与T2分期相关,更严重甚或累及壁层胸膜,则代表T3。可疑胸膜受累时,必须行弹力纤维组织化学染色辅助判断。
11. 肺内多结节癌灶:肺内多癌灶及其关系的判断对肿瘤临床分期至关重要。不同组织类型的癌灶诊断多原发,同一组织类型尤其是多发肺腺癌鉴别多原发和肺内转移则需要结合影像、形态、分子病理,并与临床多学科商议判断(弱推荐)。基层病理科应重点做到大体检查或取材勿遗漏多灶癌结节病变,给上级医院或有经验的病理中心提供规范全面的病理原始资料,以进一步会诊或明确诊断(强烈推荐)。
12. 淋巴结被膜外侵犯(extracapsular extension, ECE)的评估:2005年IASLC修订版R分类,将肿瘤ECE从R0升级为R1,但当时因数据不足未获广泛采纳。新近研究结果提示ECE患者预后与R1患者相似,ECE与局部复发的高风险相关,但与远处复发无关,ECE是术后临床制定局部控制策略的重要参考指标,尤其对N2患者影响显著,因此第9版TNM分期强调在病理报告中需明确标注是否存在ECE。但由于肺癌根治切除术清扫的淋巴结往往破碎、不完整,对被膜外侵犯难以准确评估,因此基层医院对ECE的病理评估暂不推荐。
冰冻病理诊断
由于冰冻切片的技术局限性以及受到早期肺腺癌本身存在的组织异质性等因素影响,存在冰冻病理诊断与常规病理诊断的不一致性,规范准确的冰冻病理诊断能够更好的指导手术方式。值得注意的是,参考患者的CT影像学资料,对准确取材及冰冻病理诊断均有重要指导意义,对于纯磨玻璃结节病理应谨慎诊断为浸润性腺癌。
1. 原位腺癌和微小浸润腺癌的冰冻病理诊断:正如前面相关章节所述,这两种亚型的肺癌不能在冰冻层面确诊,需待肿瘤全部取材后方可诊断,因此,对冰冻切片评估只能给出大致诊断意见。
术前CT影像学检查提示≤3 cm的磨玻璃结节,如冰冻切片上显示肿瘤细胞呈贴壁样生长,瘤细胞异型性较小,缺乏肌纤维母细胞性肿瘤间质侵犯或其他浸润癌形态,推荐结合CT影像结果纯/混杂密度磨玻璃结节诊断为“目前符合/至少为原位腺癌,需待石蜡充分取材观察最终诊断/进一步明确有无浸润”。若肿瘤可疑小灶浸润时,推荐诊断为“可疑微小浸润腺癌,需待石蜡充分取材观察最终诊断”。若可明确局部浸润(切片中浸润灶<5 mm),推荐诊断“至少微小浸润腺癌,需待石蜡充分取材观察判断浸润范围以最终明确腺癌亚型”(强烈推荐)。
2. 浸润性腺癌的冰冻病理诊断:对于影像学部分实性或实性肺结节,冰冻切片中见原位腺癌背景下的浸润成分明确>5 mm,或病灶虽小但表现为以细胞异型性明显或结构明确的浸润成分为主的腺癌,可直接诊断浸润性腺癌(强烈推荐)。
3. 肺癌与转移性癌冰冻诊断:对于同时性肺内多结节病灶,如分别可见异型性小的贴壁样生长成分,考虑为多原发腺癌,否则需要石蜡包埋后常规HE切片充分观察评估并结合必要的分子指标等因素判断多结节之间的关系(弱推荐)。如既往有其他肿瘤史,当肺内病灶出现与原肿瘤类型相似的形态时,应首先考虑转移癌可能性大,但需石蜡切片和必要的免疫组化等辅助诊断(强烈推荐)。
参考文献:
中国抗癌协会肿瘤病理专业委员会肺癌学组, 地市和县域医院肺癌病理规范化诊断共识专家组. 地市和县域肺癌病理诊断专家共识(2025版)[J]. 中华肿瘤杂志, 2025, 47(12): 1137-1151. DOI: 10.3760/cma.j.cn112152-20250428-00188
CACA:地市和县域肺癌病理诊断专家共识(2025版)
|